手性的有机硼酸化合物在合成化学和药物化学方面有着重要的应用价值。因此,发展高效的催化不对称构建方法吸引了很多化学工作者的关注。当前,利用催化不对称方法构建手性硼酸的方法主要包括过渡金属催化的烯烃的硼氢化反应、重氮化合物的硼氢插入反应、卤代烷烃的碳硼键偶联反应、a-卤代硼烷的碳碳键偶联反应和偕二硼的脱硼偶联反应。然而,这些方法均存在底物需要预先活化,这会引起额外的操作步骤且消耗更多的试剂与溶剂。因此,发展步骤和原子经济的催化不对称方法将会对这一领域的发展起到重要的推动作用。
过渡金属催化的不对称碳氢活化反应为构建手性分子提供了一条经济、简便和环境友好的途径。然而,当前的不对称碳氢键官能团化反应主要以碳碳键形成为主,碳硼键的形成反应仍然是一个极具挑战性的课题。比如,铱催化的碳氢键硼化反应是目前为止研究得最为深入的,且区域选择性控制也取得了很大的进展,但是其高效的催化不对称硼氢化反应仍然需要共价键导向,且只有两个例子。这方面研究的匮乏主要是由于缺少合适的手性配体来加速此类反应。从反应机理上而言,在铱催化的碳氢键硼化反应中有两个硼基是不参与反应的,因此有可能将其用作手性的支持配体实现不对称碳氢键硼化反应。
基于这一想法,vic115维多利亚徐森苗团队通过设计一类新型的手性双齿硼基配体,首次实现了配位键导向的过渡金属铱催化的芳基碳氢键的高效高选择性不对称硼化反应,包括去对称化反应和动力学拆分。
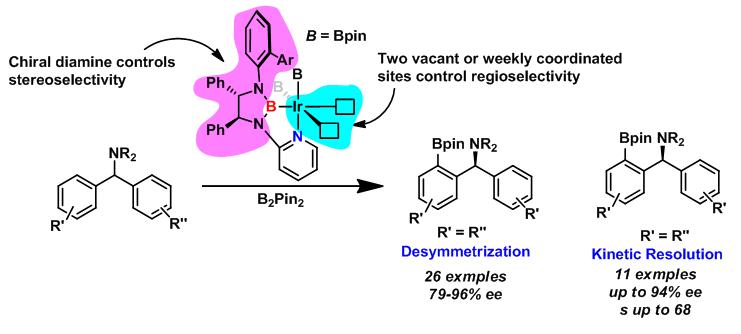
相关成果发表在近期的J. Am. Chem. Soc上 (论文链接:https://pubs.acs.org.ccindex.cn/doi/pdf/10.1021/jacs.8b13756)。
以上工作得到了国家自然科学院基金、江苏省自然科学基金、羰基合成与选择氧化国家重点实验室和杭州师范大学有机硅化学及材料技术教育部重点实验室的支持。
原文链接:http://www.nsfc.gov.cn/csc/20340/20343/36386/index.html